Lithium-Ionen-Akkumulator: Unterschied zwischen den Versionen
GHAG (Diskussion | Beiträge) K (→Herstellung) |
GHAG (Diskussion | Beiträge) |
||
| Zeile 81: | Zeile 81: | ||
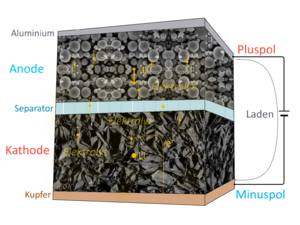
[[Datei:Lithium-Ionen-Akkumulator Laden.png|mini|Lithium-Ionen-Akkumulator Laden]] | [[Datei:Lithium-Ionen-Akkumulator Laden.png|mini|Lithium-Ionen-Akkumulator Laden]] | ||
[[Datei:Lithium-Ionen-Akkumulator Entladen.png|mini|Lithium-Ionen-Akkumulator Entladen]] | [[Datei:Lithium-Ionen-Akkumulator Entladen.png|mini|Lithium-Ionen-Akkumulator Entladen]] | ||
=== Potentiale und Wirkungsgrad === | |||
Innenwiderstand Milliohm eta 90-95% (98%) Laden bis 4,2V Entladen bis 3V | |||
=== Pluspol (positive Elektrode) === | === Pluspol (positive Elektrode) === | ||
{{Gleichung | {{Gleichung | ||
Version vom 22. Mai 2024, 08:59 Uhr
In Lithium-Ionen-Akkumulatoren basieren alle elektrochemischen Vorgänge auf der Basis von Lithium-Verbindungen. Die meisten der heute auf den Markt gebrachten lithiumbasierten Akkumulatoren enthalten Lithium-Nickel-Mangan-Cobalt-Oxide (NMC-Akkumulatoren). Die Zelle kann einen flüssigen Elektrolyten enthalten oder als Lithium-Polymer-Akkumulator ausgeführt sein. Die resultierende Zellspannung hängt vom Kathodenmaterial ab.[1]
Bei Akku-Packs kleiner und mittlerer Baugröße ist meist eine Batteriemanagement-Elektronik (BMS, mindestens Über- und Entladungsschutz) integriert. Ohne ein BMS sind die Akkus praktisch unbrauchbar.
Die häufigste Variante aufgrund des Elektrodenmaterials sind die auf Lithium-Nickel-Mangan-Cobalt-Oxiden basierenden NMC-Akkumulatoren, weitere Varianten existieren aufgrund verschiedener Elektrolyte: die Zelle kann einen flüssigen Elektrolyten enthalten oder als Lithium-Polymer-Akkumulator ausgeführt sein. Bei letzteren sind die sogenannten „Pouch“-Bauformen besonders weit verbreitet.[2]
Aufbau
Unabhängig vom Zelltyp besteht die kleinste Einheit jeder Lithium-Ionen-Zelle aus zwei Elektroden und dem Separator, der die Elektroden voneinander trennt. Dazwischen befindet sich der ionenleitfähige Elektrolyt.[3]
Lithium-Akkus sind üblicherweise in Schichtform aufgebaut, die Elektrodenmaterialien werden beidseitig auf eine Metall-Folie aufgetragen, zwischen Anoden- und Kathodenfolie kommt noch eine dritte Folie, der Separator. Diesen Folienstapel kann man dann schneiden, wickeln oder falten.
| organischer Elektrolyt | Anode | Cu-Folie 10-20 μm, Anodenpaste 100 μm |
| Separator | PE- oder PP-Membran unter 25 μm | |
| Kathode | Al-Folie 5-25 μm, Kathodepaste 40-80 μm |
Herstellung[3]
- Anodenrezeptur (Minuspol, Anode beim Entladen)
- Aktivmaterial: Graphit (90 Gew.-%)
- Leitruß: nanomikroskopischer Kohlenstoff, z.B. Super P® (5 Gew.-%)
- Lösungsmittel: Entionisiertes Wasser
- Binder: CMC (3 Gew.-%)
- Additiv: SBR (2 Gew.-%)
- Kathodenrezeptur (Pluspol, Kathode beim Entladen)
- Aktivmaterial: Li(NiMnCo)O2 (90 Gew.-%)
- Leitruß: nanomikroskopischer Kohlenstoff, z.B. Super P® (5 Gew.-%)
- Lösungsmittel: N-Methyl-2-pyrrolidon (NMP)
- Binder: PVDF (5 Gew.-%)
- Separator
- Ionendurchlässiger elektrischer Isolator
- Mikroporöse Polymermembran (PE oder PP), Keramik, Glasfaser, Kombos daraus, PET-Vlies-Keramik
- Organischer Elektrolyt
- Leitsalz: LiPF6 ca. 13 %
- Nichtwässriges Lösungsmittel: Ethylencarbonat EC, Propylencarbonat, Dimethylcarbonat DMC, Ethylmethylcarbonat EMC
- Additiv: Vinylcarbonat VC
- Außenhülle (wahlweise)
- Prismatisches/zylindrisches Metallgehäuse (Stahl oder Aluminium)
- Pouch-Folie (Aluminium-Kunststoff-Verbundfolie)
Die Herstellung der Akkupacks umfasst die drei Hauptprozesse Elektrodenfertigung, Zell-Assemblierung und Zell-Finishing.
- Elektrodenfertigung
- Mischen
- Beschichten
- Kalandern/Slitting
- Trocknen
- Zell-Assemblierung
- Vereinzeln
- Stapeln bzw. Wickeln
- Verpacken
- Elektrolytbefüllung
- Zell-Finishing
- Formierung
- Entgasung/Reifung/Test
NMC-Akkumulatoren
Lithium-Nickel-Mangan-Cobalt-Oxide, abgekürzt als Li-NMC, LNMC, NMC oder NCM bezeichnet, sind Mischoxide des Lithiums, Nickels, Mangans und des Cobalts. Sie haben die allgemeine Formel LiaNixMnyCozO2. Die wichtigsten Vertreter haben eine Zusammensetzung mit x + y + z = 1, sie zählen heute zu den wichtigsten Speichermaterialien für Lithiumionen.[4]
| Variante | Verhältnisformel | Einschätzung |
|---|---|---|
| NMC111 oder NMC333 | längst überholt | |
| NMC532 | gilt als überholt | |
| NMC622 | aktueller Stand der Technik | |
| NMC811 | kommendes Elektrodenmaterial |
Laden und Entladen
Potentiale und Wirkungsgrad
Innenwiderstand Milliohm eta 90-95% (98%) Laden bis 4,2V Entladen bis 3V
Pluspol (positive Elektrode)

|
(1) |
Minuspol (negative Elektrode)

|
(2) |
Einzelnachweise
- ↑ Lithium-Ionen-Akkumulator https://de.wikipedia.org/wiki/Lithium-Ionen-Akkumulator (abgerufen am 18.05.2024)
- ↑ Lithium-Polymer-Akkumulator https://de.wikipedia.org/wiki/Lithium-Polymer-Akkumulator (abgerufen am 18.05.2024)
- ↑ 3,0 3,1 PRODUKTIONSPROZESS EINER LITHIUM-IONEN-BATTERIEZELLE https://www.pem.rwth-aachen.de/global/show_document.asp?id=aaaaaaaaabcgujq (abgerufen am 20.05.2024)
- ↑ Lithium-Nickel-Mangan-Cobalt-Oxide https://de.wikipedia.org/wiki/Lithium-Nickel-Mangan-Cobalt-Oxide (abgerufen am 19.05.2024)