Lithium-Ionen-Akkumulator
In Lithium-Ionen-Akkumulatoren basieren alle elektrochemischen Vorgänge auf der Basis von Lithium-Verbindungen. Die meisten der heute auf den Markt gebrachten lithiumbasierten Akkumulatoren enthalten Lithium-Nickel-Mangan-Cobalt-Oxide (NMC-Akkumulatoren). Die Zelle kann einen flüssigen Elektrolyten enthalten oder als Lithium-Polymer-Akkumulator ausgeführt sein. Die resultierende Zellspannung hängt vom Kathodenmaterial ab.[1]
Bei Akku-Packs kleiner und mittlerer Baugröße ist meist eine Batteriemanagement-Elektronik (BMS, mindestens Über- und Entladungsschutz) integriert. Ohne ein BMS sind die Akkus praktisch unbrauchbar.
Die häufigste Variante aufgrund des Elektrodenmaterials sind die auf Lithium-Nickel-Mangan-Cobalt-Oxiden basierenden NMC-Akkumulatoren, weitere Varianten existieren aufgrund verschiedener Elektrolyte: die Zelle kann einen flüssigen Elektrolyten enthalten oder als Lithium-Polymer-Akkumulator ausgeführt sein. Bei letzteren sind die sogenannten „Pouch“-Bauformen besonders weit verbreitet.[2]
Aufbau
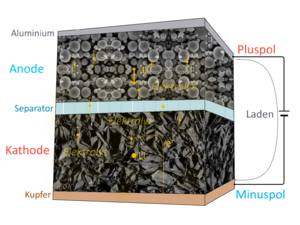
Unabhängig vom Zelltyp besteht die kleinste Einheit jeder Lithium-Ionen-Zelle aus zwei Elektroden und dem Separator, der die Elektroden voneinander trennt. Dazwischen befindet sich der ionenleitfähige Elektrolyt.[3]
Lithium-Akkus sind üblicherweise in Schichtform aufgebaut, die Elektrodenmaterialien werden beidseitig auf eine Metall-Folie aufgetragen, zwischen Anoden- und Kathodenfolie kommt noch eine dritte Folie, der Separator. Diesen Folienstapel kann man dann schneiden, wickeln oder falten.
| organischer Elektrolyt | Anode | Cu-Folie 10-20 μm, Anodenpaste 100 μm |
| Separator | PE- oder PP-Membran unter 25 μm | |
| Kathode | Al-Folie 5-25 μm, Kathodepaste 40-80 μm |
Herstellung[3]
- Anodenrezeptur (Minuspol, Anode beim Entladen)
- Aktivmaterial: Graphit (90 Gew.-%)
- Leitruß: nanomikroskopischer Kohlenstoff, z.B. Super P® (5 Gew.-%)
- Lösungsmittel: Entionisiertes Wasser
- Binder: CMC (3 Gew.-%)
- Additiv: SBR (2 Gew.-%)
- Kathodenrezeptur (Pluspol, Kathode beim Entladen)
- Aktivmaterial: Li(NiMnCo)O2 (90 Gew.-%)
- Leitruß: nanomikroskopischer Kohlenstoff, z.B. Super P® (5 Gew.-%)
- Lösungsmittel: N-Methyl-2-pyrrolidon (NMP)
- Binder: PVDF (5 Gew.-%)
- Separator
- Ionendurchlässiger elektrischer Isolator
- Mikroporöse Polymermembran (PE oder PP), Keramik, Glasfaser, Kombos daraus, PET-Vlies-Keramik
- Organischer Elektrolyt
- Leitsalz: LiPF6 ca. 13 %
- Nichtwässriges Lösungsmittel: Ethylencarbonat EC, Propylencarbonat, Dimethylcarbonat DMC, Ethylmethylcarbonat EMC
- Additiv: Vinylcarbonat VC
- Außenhülle (wahlweise)
- Prismatisches/zylindrisches Metallgehäuse (Stahl oder Aluminium)
- Pouch-Folie (Aluminium-Kunststoff-Verbundfolie)
Die Herstellung der Akkupacks umfasst die drei Hauptprozesse Elektrodenfertigung, Zell-Assemblierung und Zell-Finishing.
- Elektrodenfertigung
- Mischen
- Beschichten
- Kalandern/Slitting
- Trocknen
- Zell-Assemblierung
- Vereinzeln
- Stapeln bzw. Wickeln
- Verpacken
- Elektrolytbefüllung
- Zell-Finishing
- Formierung
- Entgasung/Reifung/Test
NMC-Akkumulatoren
Lithium-Nickel-Mangan-Cobalt-Oxide, abgekürzt als Li-NMC, LNMC, NMC oder NCM bezeichnet, sind Mischoxide des Lithiums, Nickels, Mangans und des Cobalts. Sie haben die allgemeine Formel LiaNixMnyCozO2. Die wichtigsten Vertreter haben eine Zusammensetzung mit x + y + z = 1, sie zählen heute zu den wichtigsten Speichermaterialien für Lithiumionen.[4]
| Variante | Verhältnisformel | Einschätzung |
|---|---|---|
| NMC111 oder NMC333 | längst überholt | |
| NMC532 | gilt als überholt | |
| NMC622 | aktueller Stand der Technik | |
| NMC811 | kommendes Elektrodenmaterial |
Laden und Entladen
Das Laden der Zellen darf bis etwa 4,2V erfolgen, bei höheren Spannungen setzt eine Zerstörung der Zellen durch Elektrolyse ein. Entladen darf man bis etwa 3V (andere Quellen geben 2,5 V an), ansonsten können die Zellen ebenfalls Schaden nehmen.
Pluspol (positive Elektrode)

|
(1) |
Minuspol (negative Elektrode)

|
(2) |
Potentiale
Das Normalpotential des Redoxpaares Li/Li+ beträgt unter Standardbedingungen -3,04 Volt. Durch das Elektrodenmaterial werden die Einzelpotentiale verschoben, so dass sich für die Spannung (Potentialdifferenz) ein abweichender Wert ergibt und für die gängigen NMC-Akkus bei etwa 3,7 Volt liegt.
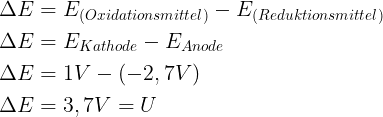
|
(3) |
Wirkungsgrad
Der Innenwiderstand der Zellen liegt im Milliohm-Bereich, die Verlust sind relativ gering, so dass sich ein Wirkungsgrad von 90-95 % ergibt. Für kleine Lade- und Entladeströme lässt sich dieser Wert auf etwa 98 % steigern.
Einzelnachweise
- ↑ Lithium-Ionen-Akkumulator https://de.wikipedia.org/wiki/Lithium-Ionen-Akkumulator (abgerufen am 18.05.2024)
- ↑ Lithium-Polymer-Akkumulator https://de.wikipedia.org/wiki/Lithium-Polymer-Akkumulator (abgerufen am 18.05.2024)
- ↑ 3,0 3,1 PRODUKTIONSPROZESS EINER LITHIUM-IONEN-BATTERIEZELLE https://www.pem.rwth-aachen.de/global/show_document.asp?id=aaaaaaaaabcgujq (abgerufen am 20.05.2024)
- ↑ Lithium-Nickel-Mangan-Cobalt-Oxide https://de.wikipedia.org/wiki/Lithium-Nickel-Mangan-Cobalt-Oxide (abgerufen am 19.05.2024)